چگونه بارهای adc با فرآیندهای سیستم تعامل دارند؟
ترکیبات آنتی بادی-دارو (ADCs) به عنوان یک کلاس انقلابی از عوامل درمانی ظهور کردهاند که ویژگی آنتیبادیهای مونوکلونال را با سمیت سلولی قوی داروهای مولکولی کوچک ترکیب میکنند. در قلب این ADC ها محموله ها هستند که نقش مهمی در تعیین کارایی و ایمنی ترکیب کلی دارند. به عنوان یک تامین کننده پیشرو محموله های ADC، ما عمیقا درگیر درک نحوه تعامل این محموله ها با فرآیندهای سیستم هستیم.
1. جذب سلولی و درونی سازی
اولین مرحله در تعامل محموله های ADC با فرآیندهای سیستم، جذب سلولی ADC است. جزء آنتی بادی مونوکلونال ADC به طور خاص به آنتی ژن های بیان شده در سطح سلول های هدف متصل می شود. این برهمکنش آنتی ژن - آنتی بادی باعث ایجاد اندوسیتوز با واسطه گیرنده می شود، فرآیندی که توسط آن ADC به داخل سلول درون اندوزوم درونی می شود [1].
هنگامی که داخل آندوزوم می شود، محیط اسیدی و حضور آنزیم های مختلف شروع به تجزیه ADC می کند. پیوند بین آنتی بادی و محموله را می توان از طریق تجزیه آنزیمی یا با هیدرولیز شیمیایی جدا کرد. به عنوان مثال، برخی از پیوندها به گونه ای طراحی شده اند که توسط پروتئازهای لیزوزومی مانند کاتپسین ها شکافته شوند. این شکاف، بار را از آنتی بادی آزاد می کند و به آن اجازه می دهد تا اثر سیتوتوکسیک خود را اعمال کند.
2. مکانیسم عمل محموله ها
انواع مختلف محموله های ADC مکانیسم های عمل مجزایی دارند. یکی از شناخته شده ترین محموله ها مونو متیل اوریستاتین E (MMAE) است. MMAE یک میکروتوبول قوی - عامل مختل کننده است. به توبولین متصل می شود و از تشکیل میکروتوبول ها جلوگیری می کند و عملکرد طبیعی دوک میتوزی را مختل می کند. این منجر به توقف چرخه سلولی در فاز G2/M می شود و در نهایت باعث القای آپوپتوز در سلول های هدف می شود [2]. شما می توانید در مورد چگونگی آن بیشتر بدانیدMonoMethyl Auristatin E عوامل ضد تومور را سنتز می کند.
محموله مهم دیگر آنسامیتوسین P - 3 است. آنسامیتوسین P - 3 دارای فعالیت ضد تومور و ضد باکتری است. با مهار پلیمریزاسیون توبولین، مشابه MMAE عمل می کند. با این حال، ساختار شیمیایی منحصر به فرد آن ممکن است قرابت های اتصال و خواص فارماکوکینتیک متفاوتی را ایجاد کند. همچنین پتانسیل هدف قرار دادن باکتری ها را دارد که آن را به یک محموله همه کاره در کاربردهای خاص تبدیل می کند. برای کسب اطلاعات بیشتر در موردآنسامیتوسین P - 3 دارای فعالیت ضد تومور و ضد باکتری است.
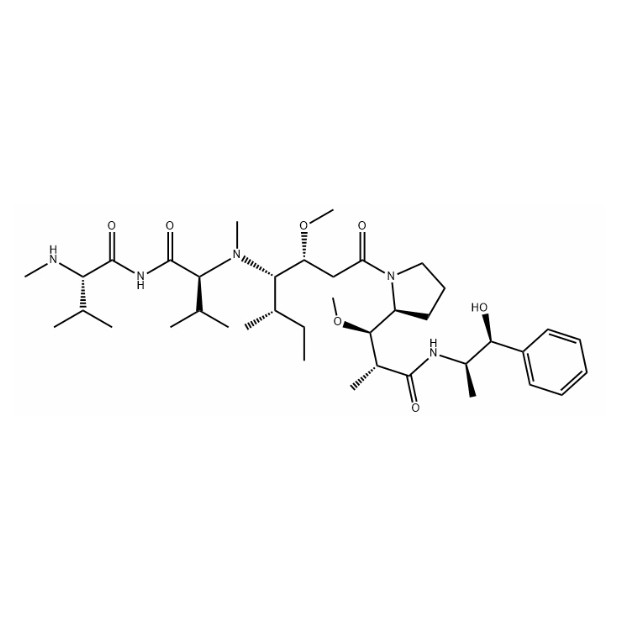
Val - Cit - PAB - MMAE یک مهارکننده کونژوگه آنتی بادی - دارو است. پیوند دهنده Val - Cit - PAB به گونه ای طراحی شده است که به طور خاص در محیط لیزوزومی سلول های هدف شکافته شود. پس از جدا شدن، MMAE آزاد می شود و سپس می تواند با ماشین های سلولی تعامل کند. این تحویل هدفمند MMAE تضمین می کند که اثر سیتوتوکسیک عمدتاً روی سلول های بیان کننده آنتی ژن اعمال می شود و سمیت خارج از هدف را کاهش می دهد. بیشتر بخوانید در موردVal - Cit - PAB - MMAE یک مهارکننده کونژوگاتور آنتی بادی است.
3. توزیع سیستمیک و فارماکوکینتیک
پس از تجویز، ADC ها از طریق جریان خون در سراسر بدن توزیع می شوند. فارماکوکینتیک ADCها و محموله های آنها تحت تأثیر عوامل متعددی از جمله اندازه ADC، پایداری پیوند دهنده و میل ترکیبی آنتی بادی به آنتی ژن هدف قرار می گیرد.
اندازه بزرگ ADC (به دلیل جزء آنتی بادی) می تواند نفوذ آن را به بافت های خاص محدود کند. با این حال، هنگامی که محموله درون سلولهای هدف آزاد میشود، اندازه کوچکتر آن به آن اجازه میدهد آزادانهتر در سلول منتشر شود و به طور بالقوه به هدف درون سلولی خود برسد. نیمه عمر ADC در جریان خون نیز یک نکته مهم است. نیمه عمر طولانی تر می تواند رهاسازی پایدارتری از محموله را فراهم کند، اما ممکن است خطر سمیت خارج از هدف را نیز افزایش دهد.

متابولیسم محمولهها میتواند در اندامهای مختلف، عمدتاً کبد، رخ دهد. آنزیم های موجود در کبد می توانند محموله ها را تغییر دهند، آنها را فعال یا غیرفعال می کنند. متابولیت های محموله ها سپس از بدن عمدتاً از طریق کلیه ها یا صفرا دفع می شوند.
4. تعامل با سیستم ایمنی
ADC ها و محموله های آنها نیز می توانند با سیستم ایمنی تعامل داشته باشند. جزء آنتی بادی ADC می تواند سلول های ایمنی را از طریق مکانیسم هایی مانند سمیت سلولی وابسته به آنتی بادی (ADCC) و سمیت سلولی وابسته به مکمل (CDC) جذب کند. ADCC شامل اتصال ناحیه Fc آنتی بادی به گیرندههای Fc روی سلولهای ایمنی مانند سلولهای کشنده طبیعی (NK) است که سپس مولکولهای سیتوتوکسیک را برای کشتن سلولهای هدف آزاد میکنند. CDC زمانی رخ می دهد که سیستم کمپلمان توسط آنتی بادی فعال می شود و منجر به تشکیل مجتمع حمله غشایی و لیز سلول های هدف می شود.
خود محموله ها نیز ممکن است اثرات تعدیل کننده ایمنی داشته باشند. برخی از محموله ها می توانند باعث آزاد شدن سیتوکین ها و کموکاین ها شوند که می توانند سلول های ایمنی را به محل تومور جذب کنند. این می تواند پاسخ ایمنی ضد تومور را افزایش دهد و به طور بالقوه کارایی درمان ADC را بهبود بخشد.
5. چالش ها و ملاحظات
با وجود پتانسیل زیاد ADC ها، چالش های متعددی در ارتباط با تعامل بارهای ADC با فرآیندهای سیستم وجود دارد. یکی از چالش های اصلی سمیت خارج از هدف است. اگر محموله در سلول های غیر هدف آزاد شود یا اگر ADC به آنتی ژن های بیان شده در سلول های طبیعی متصل شود، می تواند به بافت های سالم آسیب برساند. این می تواند منجر به عوارض جانبی مانند سمیت های خونی، آسیب کبدی و مشکلات عصبی شود.
چالش دیگر توسعه مقاومت است. سلول های سرطانی می توانند مکانیسم هایی برای فرار از اثرات سیتوتوکسیک محموله ها ایجاد کنند. به عنوان مثال، آنها میتوانند انتقالدهندههای جریان را که محمولهها را از سلولها پمپ میکنند، تنظیم کنند و غلظت درون سلولی آنها را کاهش دهند.
6. نتیجه گیری و فراخوان برای اقدام
درک نحوه تعامل بارهای ADC با فرآیندهای سیستم برای توسعه درمان های موثرتر و ایمن تر ADC بسیار مهم است. به عنوان یک تامین کننده قابل اعتماد ADC، ما متعهد به ارائه محموله های با کیفیت بالا و حمایت از تلاش های تحقیق و توسعه در این زمینه هستیم.
اگر علاقه مند به کسب اطلاعات بیشتر در مورد محموله های ADC ما هستید یا به دنبال شروع بحث خرید هستید، توصیه می کنیم با ما تماس بگیرید. تیم کارشناسان ما آماده کمک به شما در یافتن مناسب ترین محموله برای نیازهای خاص شما هستند.
مراجع
[1] داکری، ال.، و استامپ، بی. (2010). ترکیبات آنتی بادی-دارو: پیوند عوامل سیتوتوکسیک به آنتی بادی های مونوکلونال. شیمی بیوکونژوگه، 21 (1)، 5-13.
[2] فرانسیسکو، JA، Cerveny، CG، Meyer، DL، و همکاران. (2003). cAC10-vcMMAE، یک مزدوج آنتی بادی-داروی ضد CD30، باعث پسرفت بیگانهگرافتهای تومور ایجاد شده میشود. خون، 102 (4)، 1458-1465.
